Hans Krebs propuso en 1.937 que los combustibles orgánicos (piruvato) se oxidan a través de una ruta cíclica. Todos los intermediarios del ciclo son ácidos di o tri-carboxílicos, por lo que también es llamado “ciclo de los ácidos tricarboxílicos”. También se le conoce como “ciclo del ácido cítrico”.
El metabolismo oxidativo de glúcidos, grasas y proteínas, suele dividirse en 3 etapas, de las cuales el ciclo de Krebs supone la 2ª. En la 1ª etapa, los carbonos de estas macromoléculas dan lugar a moléculas de acetil-CoA de 2 carbonos, e incluye las vías catabólicas de aminoácidos (p. ej. desaminación oxidativa), la beta oxidación de ácidos grasos y la glucólisis. La tercera 3ª es la fosforilación oxidativa, en la cual el poder reductor (NADH y FADH2) generado se emplea para la síntesis de ATP según la teoría del acoplamiento quimiosmótico.
El ciclo de Krebs también proporciona precursores para muchas biomoléculas, como ciertos aminoácidos. Por ello se considera una vía anfibólica, es decir, catabólica y anabólica al mismo tiempo.
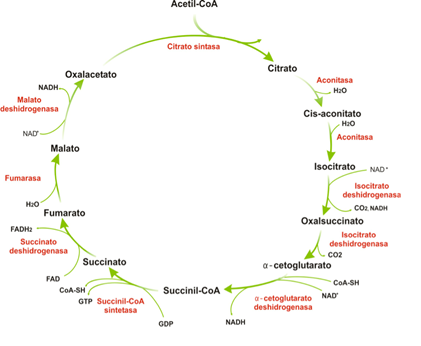
Secuencia de reacciones del ciclo de Krebs
El acetil-CoA se condensa con el oxalacetato para dar citrato, que sufre diversas transformaciones hasta llegar de nuevo a oxalacetato. Por cada acetil-CoA que entra se obtienen 2CO2, 3NADH y 1FADH2.
- El citrato se forma por condensación de acetil-CoA y oxalacetato en la reacción catalizada por la citrato sintasa.
Esta reacción también ocurre para exportar acetil-CoA al citoplasma para la síntesis de ácidos grasos y colesterol. El citrato es transportado al citoplasma por un sistema de antiporte (entra una molécula y sale otra de diferente naturaleza) donde se escinde para dar de nuevo oxalacetato y acetil-CoA, mediante la ATP-citrato liasa. El acetil-CoA se incorpora a la correspondiente ruta de biosíntesis de ácidos grasos citoplásmica y el oxalacetato retorna a la mitocondria por un sistema de lanzadera, lo que evita que se merme la anaplerosis del ciclo de Krebs.
- La segunda reacción es la isomerización del citrato en isocitrato, catalizada por la aconitasa. Realmente esto ocurre en dos pasos, entre los cuales se forma el cis-aconitato que no se disocia del centro activo. La reacción es reversible, pero el rápido consumo del isocitrato hace que transcurra en una única dirección.
- La oxidación en la que el isocitrato da lugar a oxalsuccinato está catalizada por la isocitrato deshidrogenasa. El oxalosuccinato es un intermediario inestable que permanece unido a la enzima y se descarboxila espontáneamente dando α-cetoglutarato.
La enzima isocitrato deshidrogenasa presenta dos formas en mamíferos: una forma mitocondrial, dependiente de NAD+ y que pertenece al ciclo de Krebs; y otra forma citoplásmica, responsable del suministro de NADPH y α-cetoglutarato.
- El α-cetoglutarato es sometido a una descarboxilación oxidativa por el complejo α-cetoglutarato deshidrogenasa produciendo succinil-CoA y CO2, en tres reacciones; su estructura es muy parecida a la del complejo piruvato deshidrogenasa y usa las mismas coenzimas, pero no está regulada por fosforilación/defosforilación.
Las dos oxidaciones tienen como aceptor de electrones el NAD+ en la matriz mitocondrial.
- La hidrólisis del succinil-CoA, catalizada por la succinil-CoA sintetasa (o tiokinasa), produce succinato y libera energía que se usa para la síntesis de GTP en mamíferos, o ATP en plantas y bacterias.
- La succinato deshidrogenasa, enzima asociada a la membrana interna, constituye el complejo II de la cadena respiratoria y oxida el succinato a fumarato; el cofactor que se reduce en esta reacción es el FAD.
- A continuación, el fumarato es hidratado por la fumarasa y se produce malato.
- En la última reacción del ciclo, la malato deshidrogenasa cataliza la oxidación del malato a oxalacetato, con NAD+ como aceptor de electrones.
En definitiva, hay dos entradas al ciclo: como sustrato, que se degrada a acetil-CoA y es oxidado a 2CO2; y como cebador, que llega hasta el oxalacetato.
| MOLÉCULA | ENZIMA | TIPO DE REACCIÓN | REACTIVOS/ COENZIMAS | PRODUCTOS/ COENZIMA |
| I. Citrato | 1. Aconitasa | Deshidratación | H2O | |
| II. cis-Aconitato | 2. Aconitasa | Hidratación | H2O | |
| III. Isocitrato | 3. Isocitrato deshidrogenasa | Oxidación | NAD+ | NADH + H+ |
| IV. Oxalosuccinato | 4. Isocitrato deshidrogenasa | Descarboxilación | ||
| V. α-cetoglutarato | 5. α-cetoglutarato deshidrogenasa | Descarboxilación oxidativa | NAD+ + CoA-SH | NADH + H+ + CO2 |
| VI. Succinil-CoA | 6. Succinil CoA sintetasa | Hidrólisis | GDP + Pi | GTP + CoA-SH |
| VII. Succinato | 7. Succinato deshidrogenasa | Oxidación | FAD | FADH2 |
| VIII. Fumarato | 8. Fumarato Hidratasa | Adición (H2O) | H2O | |
| IX. L-Malato | 9. Malato deshidrogenasa | Oxidación | NAD+ | NADH + H+ |
| X. Oxalacetato | 10. Citrato sintasa | Condensación |
Se han descrito transportadores específicos para ácidos di-carboxílicos (succinato, fumarato y malato); para los tri-carboxílicos (citrato, cis-aconitato e isocitrato); y para el α-cetoglutarato. Este último transportador requiere malato o succinato, puesto que es un sistema antiporte capaz de transportar el oxalacetato en determinadas circunstancias. El acetil-CoA no puede ser transportado: El piruvato, difunde rápidamente a través de la membrana interna mitocondrial. Algunos aminoácidos glucogénicos, como el glutamato y el aspartato, tienen también transportadores específicos. Estos transportadores no sólo son necesarios para importar intermediarios del ciclo al interior mitocondrial, sino también para exportarlos como precursores de otras rutas biosintéticas.
BALANCE DEL CICLO DE KREBS
- El paso final es la oxidación del ciclo de Krebs, produciendo 1 oxalacetato y 2 CO2.
- El acetil-CoA reacciona con una molécula de oxalacetato (4C) para formar citrato (6C), mediante una reacción de condensación.
- A través de una serie de reacciones, el citrato se convierte de nuevo en oxalacetato.
- Durante estas reacciones, se sacan 2C del citrato (6C) para dar oxalacetato (4C), que se liberan en forma de CO2.
- El ciclo consume netamente 1 acetil-CoA y produce 2CO2. También consume 3NAD+ y 1FAD, produciendo 3NADH + 3H+ y 1FADH2.
- Por cada molécula de piruvato, el rendimiento de un ciclo es: 1 ATP, 3NADH + 3H+, 1FADH2, 2CO2.
- Como cada glucosa (vía glucólisis) produce 2 piruvatos, tendremos un total de 2ATP, junto con 2GTP (que equivalen a 2ATP), pero ha capturado electrones energéticos en 6NADH y 2FADH2.
FUNCIONES DEL CICLO DE KREBS
El ciclo de Krebs, también conocido como el ciclo de los ácidos tricarboxílicos, fue descubierto por Hans A. Krebs y publicado por primera vez en la revista Enzymologia a finales de junio de 1937 bajo el título “The role of citric acid in intermediate metabolism in animal tissues”.
Se han estudiado las raíces evolutivas del ciclo desde los procariotas. Su aparición coincide con el establecimiento de una atmósfera aeróbica y es una ruta completamente oportunista. Antes de la aparición de organismos aeróbicos, existían diferentes fragmentos del ciclo en bacterias anaeróbicas, de manera que casi todas las reacciones ya existían. Hay consenso sobre el hecho de que estos fragmentos originariamente tenían un papel biosintético antes de aparecer el ciclo, de ahí que actualmente conserven dos funciones metabólicas básicas:
a- Catabólica. La degradación de hidratos de carbono, proteínas, grasas y cuerpos cetónicos proporcionan acetil-CoA que entra en el ciclo de Krebs y es oxidado completamente a CO2 y H2O rindiendo ATP.
b- Anabólica. Algunos de sus componentes participan en rutas como la gluconeogénesis, la lipogénesis o el metabolismo de los aminoácidos. Otros ejemplos son el ácido α-cetoglutarato (α-KG) que es precursor del glutamato, o el succinil-CoA, también precursor, del grupo hemo.
La función anabólica del ciclo de Krebs produce el drenaje del ciclo, y el material extraído debe ser repuesto por otras vías. Las rutas que aportan intermediarios al ciclo se denominan anapleróticas y los compuestos que inician un proceso bioquímico son los cebadores. El cebador básico del ciclo de Krebs es el oxalacetato, y su principal vía de formación, es la carboxilación del piruvato, catalizada por la piruvato carboxilasa (PC). Las dos funciones del ciclo sólo se pueden llevar a cabo si está bien cebado, y para la función catabólica hace falta, además, un combustible energético en abundancia.
SUSTRATOS VS CEBADORES DEL CICLO DE KREBS
El ciclo de Krebs está presente en todos los organismos eucarióticos; y, a excepción de los anaeróbicos estrictos, en la mayoría de los procarióticos, en los cuales los enzimas implicados están en el citoplasma y la función de la membrana interna mitocondrial la lleva a cabo la membrana plasmática. Dentro del grupo de los mamíferos, el ciclo de Krebs está presente en todas las células exceptuando los glóbulos rojos maduros, que carecen de mitocondrias. El funcionamiento del ciclo de Krebs depende básicamente de dos cosas: la disponibilidad de combustible energético (la fuente de acetil-CoA) y del precursor anaplerótico (la fuente de oxalacetato) (Tabla).
| Principales rutas metabólicas que proporcionan fuentes de acetil-CoA, como combustible energético mitocondrial; y de oxalacetato, como cebadores del ciclo de Krebs. | |
| Fuentes de acetil-CoA (combustible) | Fuentes de oxalacetato (cebadores) |
| Glicolisis (piruvato deshidrogenasa) | Glicolisis (piruvato carboxilasa, enzima málica) |
| β-oxidación de ácidos grasos | Catabolismo de aminoácidos glucogénicos |
| Degradación de cuerpos cetónicos | |
| Catabolismo de aminoácidos cetogénicos |
Las vías de producción de acetil-CoA, y por lo tanto, las rutas que proporcionan combustible energético en la respiración mitocondrial son: la glicolisis, que degrada a la glucosa a piruvato y éste da acetil-CoA por descarboxilación oxidativa; la β-oxidación de ácidos grasos; la combustión de cuerpos cetónicos, como el β-hidroxibutirato o el acetoacetato; y el catabolismo de aminoácidos cetogénicos. Pero además de tener una gran disponibilidad de combustible, debe haber fuentes de oxalacetato. Las rutas metabólicas capaces de proporcionar oxalacetato son: la glicolisis y el catabolismo de aminoácidos gluconeogénicos.
La descarboxilación oxidativa del piruvato a acetil-CoA es llevada a cabo por el complejo enzimático piruvato deshidrogenasa, compuesto por tres enzimas (piruvato descarboxilasa, lipoamida transacetilasa y la dihidrolipoil deshidrogenasa). En eucariotas está localizado en la matriz mitocondrial. Descarboxila el piruvato produciendo NADH, acetil-CoA y CO2. Es inhibido por el acetil-CoA.
El piruvato proveniente de la glicolisis puede ser también transformado en oxalacetato y rellenar el ciclo de Krebs por dos vías: la piruvato carboxilasa, que es un enzima mitocondrial y tiene biotina como cofactor; o por la enzima málica, que es un enzima mitocondrial.
La piruvato carboxilasa es una enzima que ya hemos nombrado anteriormente cuando vimos la gluconeogénesis. Está presente principalmente en el hígado y el páncreas, es inhibida por la insulina, evitando de esta manera la síntesis de novo de glucosa cuándo los niveles circulantes son elevados. Y, a pesar de haber investigadores que han medido la actividad de esta enzima en el músculo esquelético, ésta está ausente en este tejido. Este hecho se puede demostrar bien por el planteamiento experimental, que diferenciaba entre lo que es un sustrato del ciclo de Krebs y un cebador. De hecho, aún no está bien claro cómo se ceba el ciclo de Krebs en el músculo esquelético. Todo apunta a que lo hace el catabolismo de aminoácidos.
| Mecanismo que regula la actividad de las enzimas piruvato carboxilasa y piruvato deshidrogenasa, controlando el uso metabólico del piruvato.La piruvato deshidrogenasa (PDH) convierte el piruvato en acetil-CoA, sustrato del ciclo de Krebs, mientras que la piruvato carboxilasa lo convierte en oxalacetato, cebador del ciclo. El acetil-CoA es inhibidor alostérico de la primera enzima (efecto señalado rojo) y activador de la segunda (verde), de manera que el mecanismo garantiza que no se acumule acetil-CoA, siempre que haya suficiente cantidad de piruvato carboxilasa. Además el sistema dispone de un mecanismo adicional de seguridad para eliminar el exceso de acetil-CoA, mediante un rebosadero hacia la síntesis de cuerpos cetónicos. El piruvato procede principalmente de la glicolisis, que ocurre en el citoplasma. Todos los demás procesos representados en la figura ocurren en el interior de la mitocondria. |